Säuren – Eigenschaften, pH-Wert und Dissoziation
Säuren gehören zu den wichtigsten Verbindungsklassen in der Chemie. Sie kommen in Früchten, Reinigungsmitteln und unserem Körper vor – und haben eines gemeinsam: Sie geben in Wasser H⁺-Ionen (Protonen) ab.
Säuren im Alltag
Säuren begegnen uns täglich – oft ohne dass wir es bewusst wahrnehmen. Hier sind einige bekannte Beispiele:

- Citronensäure (\(\text{C}_6\text{H}_8\text{O}_7\)) – in Zitronen, Orangen, Limetten (saurer Geschmack)
- Äpfelsäure (\(\text{C}_4\text{H}_6\text{O}_5\)) – in Äpfeln und vielen anderen Früchten
- Weinsäure (\(\text{C}_4\text{H}_6\text{O}_6\)) – in Trauben und Wein
- Ascorbinsäure (Vitamin C) (\(\text{C}_6\text{H}_8\text{O}_6\)) – in Paprika, Beeren, Zitrusfrüchten
In Entkalkern und Haushaltsreinigern werden Säuren gezielt eingesetzt, um Kalkablagerungen (\(\text{CaCO}_3\)) aufzulösen:
\[\text{CaCO}_3 + 2\,\text{H}^+ \rightarrow \text{Ca}^{2+} + \text{H}_2\text{O} + \text{CO}_2\]Häufig eingesetzte Säure: Citronensäure – biologisch abbaubar und hautschonend.
Essigsäure

Essigsäure (Ethansäure) ist eine organische Säure mit der Summenformel \(\text{CH}_3\text{COOH}\).
- Vorkommen: Haushaltsessig enthält 5–25 % Essigsäure
- Verwendung: Konservierungsmittel in Lebensmitteln, Reinigungsmittel, Herstellung von Kunststoffen
- In Wasser dissoziiert sie teilweise (schwache Säure): \(\text{CH}_3\text{COOH} \rightleftharpoons \text{CH}_3\text{COO}^- + \text{H}^+\)
Kohlensäure
Kohlensäure (\(\text{H}_2\text{CO}_3\)) entsteht, wenn Kohlenstoffdioxid in Wasser gelöst wird – das macht Sprudelwasser „sauer":
\[\text{CO}_2 + \text{H}_2\text{O} \rightleftharpoons \text{H}_2\text{CO}_3\]Kohlensäure ist eine schwache, zweiprotonige Säure. Das Gleichgewicht liegt fast vollständig auf der linken Seite – nur wenig CO₂ liegt wirklich als H₂CO₃ vor.
Definitionen des Säurebegriffs
Den Begriff „Säure" hat die Chemie im Laufe der Zeit immer präziser gefasst. Die beiden wichtigsten Definitionen stammen von Arrhenius und Brønsted.
Eine Säure ist ein Stoff, der in wässriger Lösung H⁺-Ionen abspaltet.
Svante Arrhenius erkannte, dass saure Lösungen leitfähig sind – also Ionen enthalten. Er definierte Säuren als Verbindungen, die beim Lösen in Wasser Wasserstoff-Ionen (H⁺) freisetzen:
\[\text{HCl} \overset{\text{H}_2\text{O}}{\longrightarrow} \text{H}^+ + \text{Cl}^-\]Einschränkung
Die Arrhenius-Definition gilt nur für wässrige Lösungen. Reaktionen ohne Wasser – z. B. HCl-Gas mit Ammoniak-Gas – lassen sich damit nicht erklären.
Eine Säure ist ein Protonendonator – sie gibt ein H⁺-Ion (Proton) an eine Base ab.
Johannes Brønsted erweiterte den Säurebegriff: Eine Säure gibt immer ein Proton an einen Reaktionspartner ab, der dieses aufnimmt (= Base). Säure und Base bilden dabei ein konjugiertes Säure-Base-Paar:
\[\underbrace{\text{HCl}}_{\text{Säure}} + \underbrace{\text{H}_2\text{O}}_{\text{Base}} \rightarrow \underbrace{\text{H}_3\text{O}^+}_{\text{konj. Säure}} + \underbrace{\text{Cl}^-}_{\text{konj. Base}}\]Vorteil
Die Brønsted-Definition funktioniert auch ohne Wasser und ist allgemeiner. In der Schule verwenden wir meist diese Definition.
Vergleich der beiden Definitionen
| Arrhenius | Brønsted | |
|---|---|---|
| Säure ist … | … ein Stoff, der H⁺ in Wasser freisetzt | … ein Protonendonator |
| Bedingung | Nur in wässriger Lösung | Auch ohne Wasser möglich |
| Beispiel | \(\text{HCl} \rightarrow \text{H}^+ + \text{Cl}^-\) | \(\text{HCl} + \text{H}_2\text{O} \rightarrow \text{H}_3\text{O}^+ + \text{Cl}^-\) |
| Allgemeiner | Nein | Ja |
Versuch – Verdünnungsreihe
In diesem Versuch wird aus einer konzentrierten Salzsäure-Lösung eine Verdünnungsreihe hergestellt. Jedes Reagenzglas enthält eine um den Faktor 10 verdünntere Lösung als das vorherige.
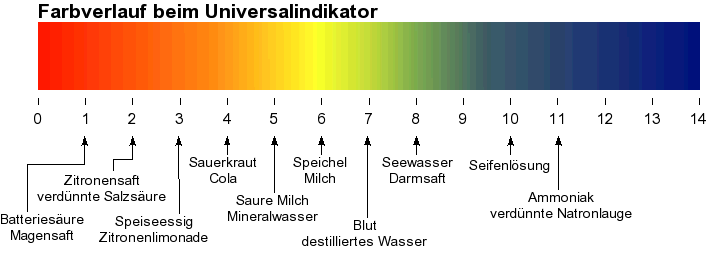
Simulation: Verdünnungsreihe mit Universalindikator
Beobachte, wie sich der Universalindikator je nach Konzentration der Salzsäure verschieden einfärbt – von dunkelrot (pH 0) bis gelb (pH 5).
Übersicht: Die 6 Reagenzgläser der Verdünnungsreihe
| Reagenzglas | Konzentration c(HCl) | pH-Wert | Farbe (Universalindikator) |
|---|---|---|---|
| RG 1 | \(10^0 = 1 \text{ mol/l}\) | 0 | Dunkelrot |
| RG 2 | \(10^{-1} = 0{,}1 \text{ mol/l}\) | 1 | Rot |
| RG 3 | \(10^{-2} = 0{,}01 \text{ mol/l}\) | 2 | Orange-Rot |
| RG 4 | \(10^{-3} = 0{,}001 \text{ mol/l}\) | 3 | Orange |
| RG 5 | \(10^{-4} = 0{,}0001 \text{ mol/l}\) | 4 | Gelb-Orange |
| RG 6 | \(10^{-5} = 0{,}00001 \text{ mol/l}\) | 5 | Gelb |
Deutung: Warum ändert sich die Farbe?
Je stärker eine Lösung verdünnt wird, desto geringer ist die Konzentration der H⁺-Ionen. Da der pH-Wert definiert ist als \(pH = -\lg[\text{H}^+]\), steigt der pH-Wert mit zunehmender Verdünnung um je eine Einheit pro Faktor 10.
Der Universalindikator reagiert auf diese unterschiedlichen H⁺-Konzentrationen mit charakteristischen Farbumschlägen – von dunkelrot (pH 0, stark sauer) über orange bis gelb (pH 5, schwach sauer). Grün entspricht dem neutralen Bereich (pH 7).
Der pH-Wert
Definition des pH-Werts
\[\boxed{pH = -\lg\left[\text{H}^+\right]}\]Der pH-Wert ist der negative dekadische Logarithmus der H⁺-Ionenkonzentration (in mol/l). Er gibt an, wie sauer oder basisch eine Lösung ist.
Eine Lösung mit einer H⁺-Konzentration von \(10^{-3} \text{ mol/l}\) hat also den pH-Wert:
\[pH = -\lg\left(10^{-3}\right) = -(-3) = 3\]pH-Skala: Säuren und Basen im Überblick
| Konzentration \([\text{H}^+]\) | pH-Wert | Einordnung | Beispiel |
|---|---|---|---|
| \(10^0 = 1 \text{ mol/l}\) | 0 | stark sauer | konzentrierte HCl |
| \(10^{-1} \text{ mol/l}\) | 1 | stark sauer | Magensäure |
| \(10^{-2} \text{ mol/l}\) | 2 | sauer | Zitronensaft |
| \(10^{-3} \text{ mol/l}\) | 3 | sauer | Essig |
| \(10^{-4} \text{ mol/l}\) | 4 | schwach sauer | Tomaten |
| \(10^{-5} \text{ mol/l}\) | 5 | schwach sauer | Kaffee |
| \(10^{-7} \text{ mol/l}\) | 7 | neutral | reines Wasser |
| \(10^{-9} \text{ mol/l}\) | 9 | schwach basisch | Backpulver-Lösung |
| \(10^{-11} \text{ mol/l}\) | 11 | basisch | Ammoniak-Lösung |
| \(10^{-13} \text{ mol/l}\) | 13 | stark basisch | Natronlauge (1 mol/l) |
| \(10^{-14} \text{ mol/l}\) | 14 | stark basisch | konzentrierte NaOH |
Dissoziationsgleichungen wichtiger Säuren
Wenn Säuren in Wasser gelöst werden, geben sie H⁺-Ionen ab – man spricht von Dissoziation. Bei starken Säuren verläuft dieser Prozess vollständig (\(\rightarrow\)), bei schwachen Säuren nur teilweise (\(\rightleftharpoons\)).
Salpetersäure → Nitrat-Ion
einprotonig, stark
\[\text{HNO}_3 \rightarrow \text{H}^+ + \text{NO}_3^-\]Salpetrige Säure → Nitrit-Ion
einprotonig, schwach
\[\text{HNO}_2 \rightleftharpoons \text{H}^+ + \text{NO}_2^-\]Kohlensäure → Hydrogencarbonat / Carbonat
zweiprotonig, schwach – 1. Stufe:
\[\text{H}_2\text{CO}_3 \rightleftharpoons \text{H}^+ + \text{HCO}_3^-\]2. Stufe:
\[\text{HCO}_3^- \rightleftharpoons \text{H}^+ + \text{CO}_3^{2-}\]Schwefelsäure → Hydrogensulfat / Sulfat
zweiprotonig – 1. Stufe (stark):
\[\text{H}_2\text{SO}_4 \rightarrow \text{H}^+ + \text{HSO}_4^-\]2. Stufe (mittelstark):
\[\text{HSO}_4^- \rightleftharpoons \text{H}^+ + \text{SO}_4^{2-}\]Schweflige Säure → Hydrogensulfit / Sulfit
zweiprotonig, schwach – 1. Stufe:
\[\text{H}_2\text{SO}_3 \rightleftharpoons \text{H}^+ + \text{HSO}_3^-\]2. Stufe:
\[\text{HSO}_3^- \rightleftharpoons \text{H}^+ + \text{SO}_3^{2-}\]Phosphorsäure → Phosphat (3 Stufen)
dreiprotonig, mittelstark – 1. Stufe:
\[\text{H}_3\text{PO}_4 \rightleftharpoons \text{H}^+ + \text{H}_2\text{PO}_4^-\]2. Stufe:
\[\text{H}_2\text{PO}_4^- \rightleftharpoons \text{H}^+ + \text{HPO}_4^{2-}\]3. Stufe:
\[\text{HPO}_4^{2-} \rightleftharpoons \text{H}^+ + \text{PO}_4^{3-}\]Merke: Starke vs. schwache Säuren
- Starke Säuren (z. B. HCl, HNO₃, H₂SO₄ 1. Stufe) dissoziieren vollständig – Pfeil zeigt nur nach rechts (\(\rightarrow\)).
- Schwache Säuren (z. B. CH₃COOH, H₂CO₃, HNO₂) dissoziieren nur teilweise – Gleichgewichtspfeil (\(\rightleftharpoons\)).
- Mehrprotonige Säuren geben ihre Protonen stufenweise ab; jede folgende Stufe ist schwächer als die vorherige.
Molekülstrukturen wichtiger Säuren
Die Strukturformeln zeigen, wie Atome im Molekül miteinander verbunden sind. Die Darstellung folgt der Oktettregel: Jedes Atom strebt eine Edelgaskonfiguration mit 8 Elektronen an.
Lewis-Strukturen der drei Säuren
Die Moleküle werden als Lewis-Strukturen dargestellt. Einfachbindungen stehen für ein gemeinsames Elektronenpaar, Doppelbindungen für zwei:
- H₂CO₃: planares Molekül, sp²-hybridisiertes C mit 1×C=O und 2×C-O-H
- H₂SO₄: tetraedrisch um S, 2×S=O und 2×S-O-H – daher nur 2 Wasserstoffatome
- H₃PO₄: tetraedrisch um P, 1×P=O und 3×P-O-H – daher 3 Wasserstoffatome
Warum gibt es für dieselbe Säure verschiedene Strukturformeln?
Die Frage, welche Strukturformel für H₂SO₄ oder H₃PO₄ „richtig" ist, beschäftigt Chemiker seit über einem Jahrhundert – und wird in Schulbüchern bis heute unterschiedlich beantwortet.
Das Lewis-Modell (1916): Gilbert N. Lewis entwickelte die Idee, dass Atome durch gemeinsame Elektronenpaare gebunden werden. Nach seiner strikten Oktettregel strebt jedes Hauptgruppenelement genau 8 Valenzelektronen an. Für Schwefelsäure bedeutet das: S bildet vier Einfachbindungen (S–O) und erfüllt damit das Oktett – trägt aber eine Formalladung von \(+2\), während zwei Sauerstoffatome je \(-1\) tragen. Formal korrekt, aber schwer intuitiv zu lesen.
Das erweiterte Oktettregel-Modell (ca. 1940–1990): Da Schwefel und Phosphor Elemente der dritten Periode sind, nahm man lange an, ihre freien 3d-Orbitale könnten zur Bindungsbildung genutzt werden. Daraus entstand das Bild von H₂SO₄ mit zwei S=O-Doppelbindungen – ohne Formalladungen, geometrisch stimmig und intuitiv einfacher. Dieses Modell verbreitete sich in Lehrbüchern weltweit.
Der moderne Blick (ab ca. 1990): Quantenmechanische Berechnungen zeigten, dass die Beteiligung der 3d-Orbitale tatsächlich minimal ist. Die Oktettregel-Darstellung mit Formalladungen ist nach heutigem Verständnis die genauere. In der Schulchemie bleibt aber oft die Doppelbindungsdarstellung üblich – sie ist einfacher und vermeidet Formalladungen, die für Schülerinnen und Schüler eine zusätzliche Hürde darstellen.
Fazit: Beide Darstellungen sind im jeweiligen Kontext vertretbar. Die hier gezeigten Lewis-Strukturen mit Doppelbindungen folgen der schulüblichen Konvention. Die Oktettregel-Strukturen mit Formalladungen sind weiter unten ergänzt.
\(\text{H}_2\text{CO}_3\)
\(\text{H}_2\text{SO}_4\)
\(\text{H}_3\text{PO}_4\)
Schwefelsäure und Phosphorsäure nach der Oktettregel
In der Oktettregel-Darstellung bildet das Zentralatom ausschließlich Einfachbindungen. Um das Oktett zu erfüllen, entstehen dabei Formalladungen – das Zentralatom gibt Ladung ab, die nicht-protonierten Sauerstoffatome nehmen sie auf.
Formalladungen in der Oktettregel-Darstellung
- \(\text{H}_2\text{SO}_4\): S trägt Formalladung \(+2\), die zwei O-Atome ohne H je \(-1\) – alle vier Bindungen sind Einfachbindungen
- \(\text{H}_3\text{PO}_4\): P trägt Formalladung \(+1\), das O-Atom ohne H trägt \(-1\) – alle vier Bindungen sind Einfachbindungen
\(\text{H}_2\text{SO}_4\) · \(\text{S}^{2+}\), 2×\(\text{O}^-\), alle Einfachbindungen
\(\text{H}_3\text{PO}_4\) · \(\text{P}^{+}\), 1×\(\text{O}^-\), alle Einfachbindungen
Teste jetzt dein Wissen!
Quiz: Säuren starten